2025年7月11日����,繼泰州站成功舉辦后��,由上海臨港聯(lián)合發(fā)展有限公司與江蘇美鳳力醫(yī)療科技有限公司聯(lián)合主辦,上海臨床創(chuàng)新轉(zhuǎn)化研究院有限公司����、上海HiMed共同協(xié)辦的美鳳力第四期"醫(yī)療器械上市及出海新路徑/新資源分享會"在上海G60科創(chuàng)云廊會客廳圓滿舉行。
作為主辦方之一���,美鳳力深感榮幸能在長三角一體化發(fā)展的核心區(qū)域舉辦此次聚焦醫(yī)療器械創(chuàng)新研發(fā)�、注冊申報及全球化布局等關鍵議題的會議���,活動匯聚了50余位長三角地區(qū)行業(yè)專家、企業(yè)代表及臨床機構負責人���,充分彰顯了長三角地區(qū)在醫(yī)療器械創(chuàng)新領域的集群優(yōu)勢���,美鳳力將持續(xù)發(fā)揮橋梁作用��,助力更多創(chuàng)新醫(yī)療器械產(chǎn)品走向市場���、邁向全球��!

在本次分享會的開幕致辭中,上海臨港松江科技城副總經(jīng)理石瀟巖先生指出���,園區(qū)聚焦"1+3"產(chǎn)業(yè)布局���,其中高端醫(yī)療器械是重點發(fā)展領域,2024年園區(qū)企業(yè)營收達1315億元����。他指出當前醫(yī)療器械行業(yè)正面臨出海新機遇,但也存在技術壁壘等挑戰(zhàn),希望通過本次與美鳳力醫(yī)療的合作���,搭建產(chǎn)業(yè)交流平臺�,助力企業(yè)把握國際市場機遇��。

隨后��,美鳳力集團董事長魏旭峰教授分享了公司"服務創(chuàng)新��、規(guī)范評價"的發(fā)展理念����,展示了六年來在創(chuàng)新醫(yī)療器械評價領域的突出成績�����,特別是完成全國1/3創(chuàng)新器械動物實驗評價的行業(yè)貢獻。魏教授重點介紹了公司構建的全球化產(chǎn)業(yè)資源網(wǎng)絡,并呼吁行業(yè)同仁把握長三角創(chuàng)新優(yōu)勢����,共同開拓國際醫(yī)療市場新機遇���。

01、醫(yī)療器械歐美上市新路徑分享—徐睿

美鳳力醫(yī)療打造全球化"一站式"出海服務平臺�����,通過中美雙實驗室模式(中國+加州)提供國際認可的GLP報告���,解決數(shù)據(jù)合規(guī)難題�。平臺整合公告機構、臨床CRO等全產(chǎn)業(yè)鏈資源,專注心血管�����、神經(jīng)介入等高值耗材領域����。實踐表明��,該平臺可幫助中國創(chuàng)新器械降低50%以上美國臨床成本,部分產(chǎn)品還能獲得醫(yī)保超額報銷����。目前已有數(shù)百家企業(yè)通過這一"技術+服務"雙出海模式成功拓展國際市場����,包括人工心臟等突破性產(chǎn)品。
02��、創(chuàng)新器械海外臨床試驗新資源分享—鄧曉宇

中國醫(yī)療器械出海正呈現(xiàn)全球化趨勢�,但各領域節(jié)奏不一�����。數(shù)據(jù)顯示�����,僅8%出海企業(yè)能真正在海外市場獲得成功�,這些企業(yè)通常具備兩大特征:一是由CEO/董事長直接牽頭海外戰(zhàn)略��,二是產(chǎn)品具有顯著創(chuàng)新性���。歐美市場雖規(guī)模不及中國,但定價高�、競爭少����,東南亞則消費意愿強。產(chǎn)品出海決策應基于臨床價值而非單純市場份額預測�,建議企業(yè)結(jié)合創(chuàng)新性與市場需求綜合判斷����。美鳳力平臺型企業(yè)通過整合全球資源�,正在幫助中國器械企業(yè)突破出海瓶頸���,實現(xiàn)從研發(fā)到商業(yè)化的全鏈條支持�。
03��、港澳及東南亞產(chǎn)品上市新資源分享—鄧南天

中國醫(yī)療器械出海正呈現(xiàn)全球化趨勢,但各領域節(jié)奏不一����。數(shù)據(jù)顯示,僅8%出海企業(yè)能真正在海外市場獲得成功��,這些企業(yè)通常具備兩大特征:一是由CEO/董事長直接牽頭海外戰(zhàn)略,二是產(chǎn)品具有顯著創(chuàng)新性�����。歐美市場雖規(guī)模不及中國,但定價高����、競爭少����,東南亞則消費意愿強����。產(chǎn)品出海決策應基于臨床價值而非單純市場份額預測,建議企業(yè)結(jié)合創(chuàng)新性與市場需求綜合判斷。美鳳力平臺型企業(yè)通過整合全球資源��,正在幫助中國器械企業(yè)突破出海瓶頸��,實現(xiàn)從研發(fā)到商業(yè)化的全鏈條支持�����。
04�、中美貿(mào)易戰(zhàn)下��,醫(yī)療器械輸美的機遇和挑戰(zhàn)—Tracy Teng

美國仍是中國醫(yī)械出口最大市場(占出口總24%)���,2024年進口醫(yī)械超2600萬批次���。當前需關注:1)特朗普2.0政策下FDA審批或更靈活;2)行業(yè)關稅調(diào)整(部分品類達50-600%)�;3)510K審批平均需209天����;4)美代必須24小時響應FDA要求(曾有企業(yè)因失聯(lián)被罰360萬美元)����;5)FDA實施"飛行檢查"新規(guī)(取消提前通知)。建議企業(yè)建立符合QS820的質(zhì)量體系�,做好全生命周期合規(guī)管理�����。團隊已服務超5000家企業(yè)�����,提供從注冊到上市后監(jiān)管的一站式解決方案。
05、歐盟認證常見問題解析及快速認證路徑分享—張惠
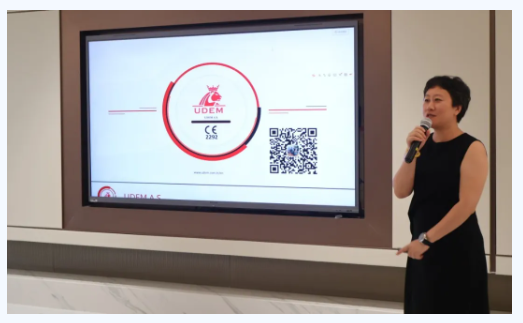
當前MDR認證通過率僅33%(申請10554件/發(fā)證3511件),高風險產(chǎn)品通過率不足4%�����。認證周期普遍需12-24個月,其中三類產(chǎn)品因需CCP臨床評估(最長60天)耗時更久���。建議企業(yè)重點關注:1)27年底MDD證書到期前的窗口期;2)認證機構選擇標準(審核資源/服務模式)��;3)臨床評價替代方案(真實世界數(shù)據(jù)可縮短50%周期)�����。團隊已建立50+專家審核網(wǎng)絡,提供從技術文件準備到現(xiàn)場審核的全流程服務��,最快14個月完成三類產(chǎn)品認證�。特別提醒:企業(yè)需提前2年規(guī)劃高風險產(chǎn)品認證路徑���,避免市場空窗期���。
06、醫(yī)保掛網(wǎng)準入助力創(chuàng)新醫(yī)療器械發(fā)展—伊貴銘

前全國統(tǒng)一招采平臺已實現(xiàn)價格透明化�,企業(yè)需特別注意:1)備案采購≠陽光采購�����,概念混淆將導致產(chǎn)品無法入院�����;2)價格聯(lián)動機制下��,單省定價失誤將引發(fā)全國性風險(曾有65億規(guī)模企業(yè)因此退出市場);3)產(chǎn)品分類直接影響集采分組�,如人工韌帶需明確是否歸入骨科耗材基材目錄���。建議企業(yè)建立專業(yè)團隊�,在申報前完成:①全國價格大數(shù)據(jù)分析����;②產(chǎn)品精準分類定位�;③報價策略模擬(誤差可能導致產(chǎn)品永久限價)��。團隊已構建智能監(jiān)測系統(tǒng)�,可提前預警價格風險�,協(xié)助企業(yè)合規(guī)準入。
07��、上海臨轉(zhuǎn)院在臨床轉(zhuǎn)化促進產(chǎn)業(yè)發(fā)展的探索與案例—王立言

上海臨床創(chuàng)新轉(zhuǎn)化研究院作為市級醫(yī)療創(chuàng)新服務平臺,重點推動三甲醫(yī)院臨床研究與成果轉(zhuǎn)化�。平臺已打通醫(yī)院持股路徑(如與十院合作成立微生態(tài)企業(yè))����,并設立3億元專項基金支持醫(yī)工轉(zhuǎn)化項目�����。依托申康中心管理的38家醫(yī)院資源,平臺可提供:1)臨床需求對接服務(已挖掘400+院內(nèi)項目)�;2)加速倫理審查與患者招募;3)醫(yī)療數(shù)據(jù)合規(guī)應用(覆蓋醫(yī)保/自費患者全診療數(shù)據(jù))�����。通過"行政+市場"雙輪驅(qū)動��,助力企業(yè)實現(xiàn)從臨床需求到產(chǎn)業(yè)化的高效轉(zhuǎn)化�,目標將醫(yī)院轉(zhuǎn)化收入占比提升至20%�。
會議最后,上海臨港松江科技城總經(jīng)理薛酉天先生作總結(jié)發(fā)言時指出���,園區(qū)醫(yī)療器械產(chǎn)業(yè)已形成完整生態(tài)鏈����,入駐企業(yè)突破130家。依托臨港集團雄厚的產(chǎn)業(yè)資源����,園區(qū)將與美鳳力等專業(yè)機構深度合作��,推出包括'專利快審'(3-6個月)和'司法保護聯(lián)動機制'在內(nèi)的特色服務,全力支持企業(yè)成長���。

至此�,美鳳力"器械藥品�����、醫(yī)療器械上市及出海新路徑/新資源"泰州���、上海雙城系列活動圓滿收官���。作為扎根長三角的醫(yī)療科技服務平臺��,美鳳力將持續(xù)發(fā)揮橋梁作用����,整合全球資源����,助力更多創(chuàng)新醫(yī)療器械產(chǎn)品走向市場、邁向國際。讓我們共同期待下一次的相聚���,攜手開創(chuàng)中國醫(yī)療器械產(chǎn)業(yè)高質(zhì)量發(fā)展的新篇章!
美鳳力借多年的大動物經(jīng)驗,堅持以“務實求真”為宗旨�,累計為4000多家客戶提供品質(zhì)大動物臨床前服務,得到了客戶的一致好評�����。如果您有動物試驗��、臨床培訓、組織病理����、大動物試驗、臨床試驗�����、產(chǎn)品注冊科研課題等...
請立即點擊咨詢我們或撥打咨詢熱線: 17312606166 ��,我們會詳細為你一一解答你心中的疑難���。 添加好友




 17312606166
17312606166