糖尿病性心肌病(DCM)被定義為糖尿病患者在沒(méi)有高血壓��、冠狀動(dòng)脈疾病或明顯瓣膜疾病的情況下��,與左心室功能障礙相關(guān)的病理生理狀態(tài)����。其特點(diǎn)為早期左室肥大��、間質(zhì)纖維化�����、糖尿病微血管病變及相關(guān)的異常舒張功能障礙����,以及左室射血分?jǐn)?shù)降低���,最終導(dǎo)致心力衰竭。DCM的病理過(guò)程包括全身性胰島素抵抗��、能量代謝紊亂����、線粒體功能障礙����、氧化應(yīng)激增加、鈣處理不當(dāng)和炎癥���。然而,對(duì)于DCM的治療尚無(wú)具體的策略��。
線粒體是心臟能量代謝的主要部位�。線粒體功能的改變是導(dǎo)致DCM的主要原因。生理上,細(xì)胞內(nèi)三磷酸腺苷(ATP)由各種能量底物產(chǎn)生��,用于心臟功能;40-60%的ATP由脂肪酸的β-氧化產(chǎn)生(FAO)���, 10%-20%由丙酮酸(葡萄糖和乳酸)產(chǎn)生����,2%-8%由酮體和氨基酸產(chǎn)生�。然而,隨著糖尿病的發(fā)展����,心臟胰島素抵抗和高脂血癥抑制了葡萄糖的利用�����,導(dǎo)致90%-100%的FAO無(wú)法滿足人體的能量需求���,從而導(dǎo)致嚴(yán)重的心臟脂肪毒性,降低了能量生產(chǎn)的靈活性和效率���。
線粒體通過(guò)生物發(fā)生、融合和裂變等一系列動(dòng)態(tài)過(guò)程改變形態(tài)���,以響應(yīng)高能量需求�,這被稱為線粒體動(dòng)力學(xué)。動(dòng)力蛋白相關(guān)蛋白1 (Drp1)和裂變蛋白1 (Fis1)是參與線粒體裂變反應(yīng)的主要蛋白���。線粒體內(nèi)外膜的融合事件由有絲分裂蛋白1/2 (Mfn1/Mfn2)和視神經(jīng)萎縮蛋白1 (Opa1)驅(qū)動(dòng)。在DCM患者和動(dòng)物模型的心臟中觀察到異常的線粒體動(dòng)力學(xué)���。
泛素化是一種重要的翻譯后修飾�����,由E3泛素連接酶介導(dǎo)�����,它將泛素分子結(jié)合到靶蛋白底物上��,隨后被蛋白酶體識(shí)別并降解���。去泛素化是與泛素化相反的過(guò)程��。這兩個(gè)事件維持著動(dòng)態(tài)平衡,調(diào)節(jié)著體內(nèi)重要的生物過(guò)程����。泛素特異性蛋白酶7 (USP7)�,也被稱為皰疹病毒相關(guān)泛素特異性蛋白酶(HAUSP)��,是去泛素酶最大亞家族——泛素特異性蛋白酶(USP)家族的成員���。
據(jù)報(bào)道�����,USP7與多種心血管疾病有關(guān)�。如擴(kuò)張型心肌病患者左心室USP7異常升高�,通過(guò)去泛素化修飾P53介導(dǎo)心臟損害的發(fā)生;USP7通過(guò)Sp1/Sp3-Notch1軸介導(dǎo)內(nèi)皮細(xì)胞的病理生理性血管生成;USP7受miR-409-5p的負(fù)調(diào)控,miR-409-5p在缺血/再灌注小鼠心臟中通過(guò)p53/TfR1信號(hào)通路介導(dǎo)鐵凋亡;此外����,SIRT1/USP7軸介導(dǎo)阿霉素誘導(dǎo)的老年小鼠心臟毒����。然而����,USP7在DCM患者心臟能量代謝中的關(guān)鍵作用尚未報(bào)道�����。因此��,它們被認(rèn)為是代謝和心臟疾病有價(jià)值的治療靶點(diǎn)。

圖片來(lái)源:https://doi.org/10.1016/j.phrs.2024.107235
近日��,來(lái)自廣東省中西醫(yī)結(jié)合代謝性疾病研究中心的研究者們?cè)赑harmacol Res雜志上發(fā)表了題為“USP7 promotes cardiometabolic disorders and mitochondrial homeostasis dysfunction in diabetic mice via stabilizing PGC1β”的文章,該研究揭示了USP7通過(guò)穩(wěn)定PGC1β促進(jìn)糖尿病小鼠心臟代謝紊亂和線粒體穩(wěn)態(tài)功能障礙����,提出了一種對(duì)糖尿病小鼠的心臟發(fā)保護(hù)作用的策略。
糖尿病性心肌病(DCM)是糖尿病的主要并發(fā)癥��,以左心室功能障礙為特征。目前��,對(duì)DCM缺乏有效的治療方法�。泛素特異性蛋白酶7 (USP7)在多種疾病中起關(guān)鍵作用。但USP7是否參與DCM尚未確定�����。
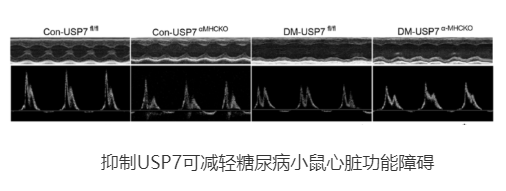
圖片來(lái)源:https://doi.org/10.1016/j.phrs.2024.107235
在這項(xiàng)研究中,研究者證明了USP7在糖尿病小鼠心臟和與HG+PA共同處理的nmcm或與PA共同處理的H9c2細(xì)胞中上調(diào)��。通過(guò)條件基因敲除或化學(xué)抑制USP7沉默���,可以逆轉(zhuǎn)糖尿病心臟形態(tài)和功能的異常。蛋白質(zhì)組學(xué)分析結(jié)合生化驗(yàn)證證實(shí)PCG1β是USP7的直接蛋白底物之一����,并通過(guò)共激活PPARα信號(hào)通路加重心肌損傷。USP7沉默通過(guò)抑制線粒體裂變和促進(jìn)融合事件�����,恢復(fù)脂肪酸代謝相關(guān)蛋白的表達(dá),恢復(fù)線粒體穩(wěn)態(tài)��。在體外也觀察到類似的效果�����。該研究數(shù)據(jù)表明��,USP7通過(guò)穩(wěn)定PCG1β促進(jìn)心臟代謝紊亂和線粒體穩(wěn)態(tài)功能障礙�����,這表明沉默USP7可能是一種治療DCM的策略����。
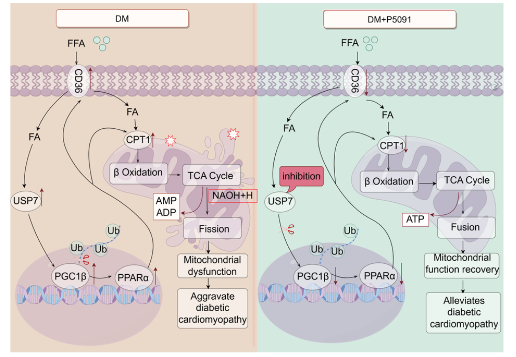
USP7/PGC1β軸介導(dǎo)糖尿病小鼠心臟DCM病理過(guò)程的圖形摘要
圖片來(lái)源:https://doi.org/10.1016/j.phrs.2024.107235
綜上所述����,USP7沉默通過(guò)去泛素化調(diào)節(jié)PGC-1β介導(dǎo)的心臟代謝和線粒體穩(wěn)態(tài)�����,對(duì)糖尿病小鼠的心臟發(fā)揮心臟保護(hù)作用��。
參考文獻(xiàn)
Meiling Yan et al. USP7 promotes cardiometabolic disorders and mitochondrial homeostasis dysfunction in diabetic mice via stabilizing PGC1β. Pharmacol Res. 2024 May 28:205:107235. doi: 10.1016/j.phrs.2024.107235.




 17312606166
17312606166