上海交通大學(xué)醫(yī)學(xué)院松江研究院/中國(guó)科學(xué)院腦科學(xué)與智能技術(shù)卓越創(chuàng)新中心(神經(jīng)科學(xué)研究所)仇子龍團(tuán)隊(duì)與復(fù)旦大學(xué)腦科學(xué)轉(zhuǎn)化研究院程田林團(tuán)隊(duì)合作���,在神經(jīng)科學(xué)國(guó)際權(quán)威期刊NatureNeuroscience上發(fā)表了題為:Whole-braininvivobaseeditingreversesbehavioralchangesinMef2cmutantmice的研究論文。
該研究首次報(bào)道了在全腦范圍內(nèi)利用單堿基編輯技術(shù),成功改善MEF2C孤獨(dú)癥小鼠模型神經(jīng)發(fā)育與孤獨(dú)癥樣核心行為表型���。

仇子龍研究團(tuán)隊(duì)通過全外顯子組測(cè)序技術(shù)在一例中國(guó)的孤獨(dú)癥患兒的MEF2C基因上發(fā)現(xiàn)了一個(gè)新發(fā)點(diǎn)突變(denovomutation)���,c.T104C,p.L35P,MEF2C基因已被證實(shí)是一個(gè)很重要的孤獨(dú)癥風(fēng)險(xiǎn)基因�����,突變會(huì)導(dǎo)致神經(jīng)發(fā)育遲滯及一系列嚴(yán)重癥狀�,但是該新發(fā)點(diǎn)突變對(duì)于MEF2C基因功能的影響未知�。
研究團(tuán)隊(duì)首先利用分子細(xì)胞生物學(xué)的研究方法在體外探究了L35P點(diǎn)突變對(duì)MEF2C蛋白結(jié)構(gòu)���、表達(dá)以及功能上的影響及其分子機(jī)制(圖I和圖II)���。研究團(tuán)隊(duì)發(fā)現(xiàn)L35P突變會(huì)導(dǎo)致MEF2C蛋白質(zhì)發(fā)生依賴泛素化蛋白酶體途徑的快速降解(圖II),最終顯著降低MEF2C蛋白的表達(dá)水平(圖I)����。
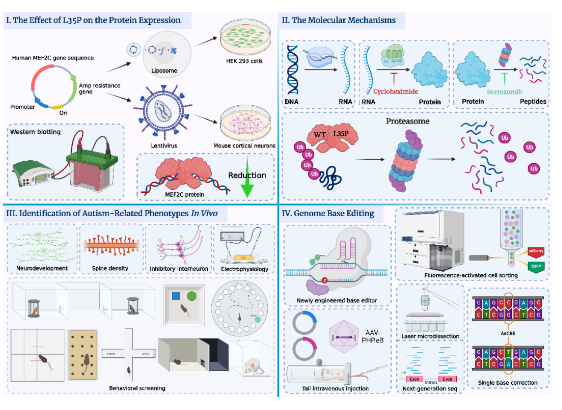
圖I:L35P點(diǎn)突變會(huì)顯著降低MEF2C蛋白表達(dá)水平���。
圖II:L35P點(diǎn)突變會(huì)通過泛素化蛋白酶體降解途徑介導(dǎo)MEF2C蛋白翻譯后快速降解���,且表現(xiàn)出dominantnegativeeffect。
圖III:Mef2cL35P雜合小鼠表現(xiàn)出與孤獨(dú)癥相關(guān)的異常神經(jīng)發(fā)育,突觸密度降低����,抑制性中間神經(jīng)元數(shù)量下降及異常的電生理表型����,且會(huì)出現(xiàn)孤獨(dú)癥相關(guān)的行為學(xué)表型�����。
圖IV:基于CRISPR/Cas9系統(tǒng)開發(fā)的新型胞嘧啶單堿基編輯系統(tǒng),通過體內(nèi)及體外驗(yàn)證了其在目標(biāo)靶點(diǎn)的堿基編輯效率以及脫靶事件����,證明該系統(tǒng)是高效�,準(zhǔn)確且安全的。
為了研究L35P基因突變對(duì)小鼠行為學(xué)表型的影響����,研究團(tuán)隊(duì)構(gòu)建了Mef2cL35P點(diǎn)突變敲入小鼠模型,并通過生物化學(xué)���、免疫熒光成像以及行為學(xué)實(shí)驗(yàn)探究了其神經(jīng)發(fā)育及行為學(xué)表型�����。研究發(fā)現(xiàn)Mef2cL35P雜合突變小鼠大腦中存在孤獨(dú)癥相關(guān)的神經(jīng)生理學(xué)特征以及發(fā)育異?���,F(xiàn)象�����,并且表現(xiàn)出社交障礙以及刻板行為等孤獨(dú)癥核心癥狀的行為學(xué)表型(圖III)。
隨后,為了修復(fù)小鼠大腦神經(jīng)元中的L35P點(diǎn)突變�����,仇子龍和程田林團(tuán)隊(duì)合作開發(fā)了一種基于CRISPR-Cas9的新型胞嘧啶單堿基編輯系統(tǒng)(APOBEC3AembeddingCytosineBaseEditor,AeCBE)�,使其能夠?qū)⑿∈驧ef2c基因中特定位置上異常的C·G堿基對(duì)轉(zhuǎn)換成正常的T·A堿基對(duì)�����。
為了能夠使得AeCBE系統(tǒng)成功地跨越小鼠血腦屏障(BBB)�,研究團(tuán)隊(duì)將AeCBE系統(tǒng)包裝進(jìn)PHP.eB血清型腺相關(guān)病毒(AAV)中�,并且利用單次小鼠尾靜脈注射AAV的遞送方式���,使得AeCBE系統(tǒng)在小鼠大腦中得以成功表達(dá)。經(jīng)AeCBE系統(tǒng)編輯后,研究團(tuán)隊(duì)在體內(nèi)檢測(cè)到較高的單堿基編輯效率以及低脫靶事件�����,驗(yàn)證了新開發(fā)的AeCBE系統(tǒng)具備高效性�、準(zhǔn)確性且安全性的特點(diǎn)(圖IV)�。
最后�����,研究團(tuán)隊(duì)檢測(cè)了經(jīng)過AeCBE堿基編輯系統(tǒng)介導(dǎo)的基因治療后Mef2cL35P突變雜合小鼠大腦中的神經(jīng)生理學(xué)變化以及行為學(xué)表型��。在經(jīng)過單堿基編輯技術(shù)介導(dǎo)的基因修復(fù)后���,研究團(tuán)隊(duì)發(fā)現(xiàn)Mef2cL35P突變雜合小鼠大腦中降低的Mef2c蛋白表達(dá)水平得到恢復(fù)����,并且其社交障礙以及重復(fù)刻板性行為也得到了明顯的改善��。
總的來說,該研究提出了一種利用CRISPR-Cas9介導(dǎo)的單堿基編輯系統(tǒng)在全腦水平修復(fù)致病基因單核苷酸突變的體內(nèi)基因編輯策略��,從而為各種大腦遺傳疾病提供新的治療方案和思路。
上海交通大學(xué)醫(yī)學(xué)院松江研究院/中國(guó)科學(xué)院腦智卓越中心仇子龍研究員和復(fù)旦大學(xué)腦科學(xué)轉(zhuǎn)化研究院程田林研究員為該論文共同通訊作者�。中國(guó)科學(xué)院腦智卓越中心李維克博士�����、復(fù)旦大學(xué)腦科學(xué)轉(zhuǎn)化研究院博士生張淑倩為該論文共同第一作者�����。




 17312606166
17312606166